국내 29개 품목 허가..효능 논란 이후 임상재평가 결과 절반만 생존
최근 최순실 국정농단 사태에서 난데없이 태반주사가 등장했다. 박근혜 대통령이 청와대에서 태반주사를 맞았다는 의혹이 불거지면서 태반주사의 효능에 대한 궁금증이 커지고 있다.
◇인태반의약품 3종류로 구분..제품마다 원료ㆍ적응증 달라
사람 태반으로 만드는 인태반 의약품은 크게 자하거추출물, 자하거가수분해물, 자하거엑스복합제 등 세 가지로 구분된다. 여기서 자하거는 건강한 산모의 태반을 말한다. 현재 식약처로부터 허가받고 판매 중인 의약품은 총 29개 품목(국내 판매 불가한 수출용 허가 4개 제외)이다.
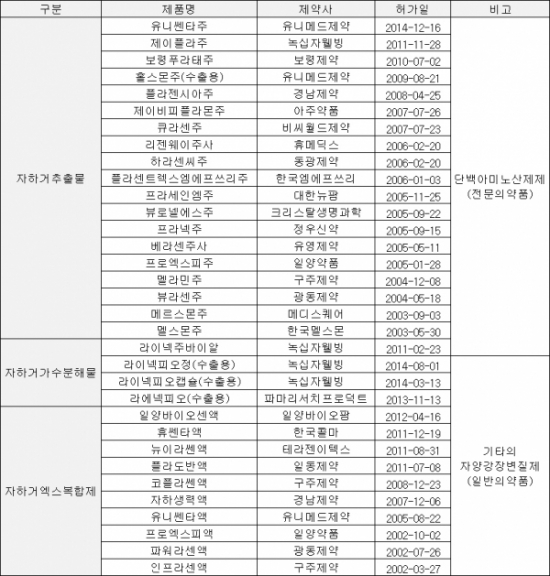
자하거추출물과 자하거가수분해물은 의사 처방을 받고 피하주사를 맞는 주사제다. 자하거엑스복합제는 약국에서 구매할 수 있는 드링크 제품이다.
자하거추출물의 경우 미황색의 투명한 액을 담고 있는 갈색 앰플 주사제로 1회 2 ml, 1주일에 3회씩 2주간(총 6회) 피하주사 하도록 허가받았다. 자하거가수분해물은 담황갈색 또는 황갈색의 투명한 액이 갈색 앰플에 들어있는 주사제다.
자하거추출물과 자하거가수분해물은 원료와 제조공정이 다르다.
자하거추출물은 태반을 가수분해하는 방식으로 만든다. 태반을 염산에 녹이면 저분자 아미노산이 나오는데 이 물질이 자하거추출물이다. 태반주사의 초기 모델로 식약처가 인정한 효능은 ‘갱년기 장애 증상의 개선’이다.
자하거가수분해물은 태반 뿐만 아니라 제대(탯줄), 양막을 원료로 제조한다. 태반, 제대, 양막을 아세톤으로 탈지해 불순물을 제거한 다음 건조시킨다. 이후 펩신으로 가수분해해 중분자 아미노산을 뽑아낸 다음 자하거추출물 공정에 사용하는 염산 가수분해를 통해 저분자 아미노산을 만들어낸다. 자하거가수분해물은 중분자 아미노산과 저분자 아미노산이 포함된 제품이다.
자하거추출물에 비해 원료도 다양하고 제조공정이 복잡해 진보된 태반주사로 평가받는다. 원가도 상대적으로 비싼 것으로 알려졌다. 자하거가수분해물은 자하거추출물과는 달리 ‘만성간질환에 있어서의 간기능의 개선’ 효능을 인정받았다. 국내에서는 녹십자웰빙의 '라이넥'이 유일한 자하거가수분해물 제품이다. 박근혜 대통령은 ‘라이넥’을 투여받은 것으로 알려졌는데, 허가된 적응증에 따라 투여받았다면 간기능 개선을 목적으로 사용했다는 얘기가 된다.
흔히 태반드링크로 불리는 자하거엑스복합제는 갈색유리병에 들어 있는 진한 갈색의 액제로 자양강장, 허약체질, 육체피로, 병후의 체력저하, 식욕부진 효능을 인정받았다. 자하거엑스복합제는 자하거엑스 1.5ml~7.5ml과 함께 카페인무수물·티아민질산염·피리독신염산염 등도 함유했다. 나머지 성분들은 자양강장제로 많이 마시는 박카스와 구성 성분이 유사하다. 마시는 자양강장제에 자하거추출물 극미량을 넣었다고 보면 된다.
인태반 의약품은 다른 의약품과 마찬가지로 부작용 발생 가능성이 있다.
자하거추출물은 쇼크, 오한, 구역, 발열, 발적, 발진 등이 발생할 수 있고 동통, 발적, 유방통, 여성형 유방이 나타날 수 있다는 내용이 허가사항에 명시됐다. 자하거가수분해물도 자하거추출물과 사용상 주의사항은 유사하다. 자하거엑스복합제는 구역, 구토, 묽은 변, 속쓰림 등의 부작용 가능성이 있다.
◇보건당국, 10년 전 인태반의약품 전 제품 임상재평가..절반 퇴출
‘회춘 주사’로도 불리는 태반 주사는 한때 일부 중년 여성들 사이에 마치 만병통치약으로 인식되며 크게 유행했다. 정식 처방을 받지 않고 밀거래를 통해 유통되며 사회적 문제를 야기하기도 했다. 인태반의약품의 효능에 의구심을 갖는 시선도 많았다.
급기야 지난 2006년 식품의약품안전처(당시 식약청)는 시중에 판매 중인 인태반 의약품의 효능을 점검하겠다며 전 제품에 대해 임상시험을 진행하고 효능 검증 자료를 제출할 것을 지시했다.
지난 2011년 약 5년에 걸쳐 진행된 임상재평가 결과가 발표됐는데 당초 검증 대상 46개 품목 중 를 절반에 불과한 23개 품목만 효능을 인정받고 판매가 허용됐다.
자하거추출물은 27개 중 17개가 유용성을 인정받고 생존에 성공했다. 녹십자, 유니메드, 진양제약 등이 판매 중이던 4개 품목은 유용성을 인정받지 못해 허가가 취소됐고 당시 유통 중인 제품은 강제회수 조치됐다. 대화제약, 비티오제약, JW신약, KMS제약, 하나제약, 휴온스 제약 등은 재평가를 받지 않고 허가를 자진 취하하며 시장에서 사라졌다.
자하거가수분해물은 재평가 대상 9개 품목 중 지씨제이비피(현 녹십자웰빙)의 ‘라이넥’ 1개 품목만 판매가 허용됐다. 광동제약, 대원제약, 경남제약 등의 제품은 효능 인정에 실패해 허가가 취소됐고 구주제약, 드림파마는 자료를 제출하지 않아 허가가 취소됐다. 동광제약, 한국BMI, 지씨제이비피 등은 허가를 취하했다.
인태반의약품의 임상재평가 과정에서 적잖은 잡음을 노출했다. 허가를 자진취하한 제품 중 일부는 임상시험을 진행했지만 당초 목표로 설정한 효능이 나타나지 않아 자료제출 마감일 직전에 허가를 취하한 것으로 알려졌다. 제약사들은 식약처가 과도한 효능 검증 기준을 제시할 것을 요구한다는 불만도 팽배했다. 태반드링크와 같은 일반의약품의 경우 임상시험을 통해 효능 자료 제출을 요구하는 것은 흔치 않다.
한 식약처 전직 공무원은 “인태반 의약품이 마치 만병통치약인 것처럼 유행하며 오남용이 심각했다. 당시 시중에 판매 중인 제품 중 효과가 없는 제품은 퇴출시키자는 의도로 엄격한 기준의 임상재평가 자료를 제출할 것을 요구했다”고 말했다.











![요즘 가요계선 '역주행'이 대세?…윤수일 '아파트'→키오프 '이글루'까지 [이슈크래커]](https://img.etoday.co.kr/crop/320/200/2099221.jpg)