대웅제약은 보툴리눔 톡신 제제 ‘나보타’의 미국 3상 임상 결과가 국제학술지 ‘더마톨로직 서저리(Dermatologic Surgery)’에 게재됐다고 25일 밝혔다.
나보타는 미국에서 654명의 미간주름 환자를 대상으로 3상 임상(EV-001, EV-002)을 두 차례 진행했다. 만 18세 이상의 중등증 또는 중증 미간주름 환자를 대상으로 나보타와 위약을 동일 용량으로 1회 투여하고, 일정시점 이후 4단계 미간주름스케일(Glabellar Line Scale·GLS)을 활용해 주름개선 효과를 확인하는 이중맹검 방법으로 했다.
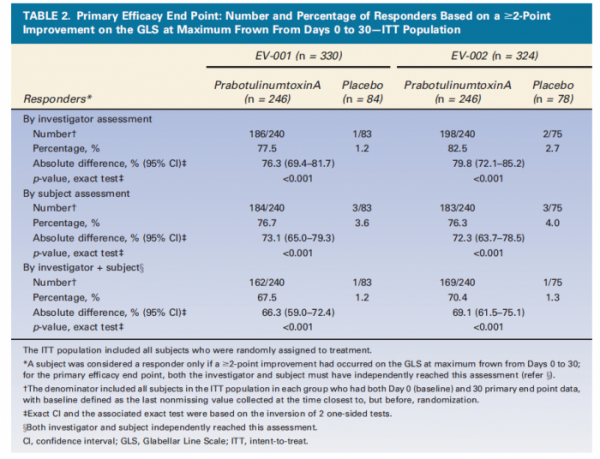
두 차례 임상에서 시술 후 30일째, 총 4단계 GLS 중 연구자와 피험자가 동시에 2단계 이상 주름이 개선됐다고 응답한 비율이 각각 67.5%와 70.4%로 나타났다. 이는 위약군에서의 해당 응답 비율인 1.2%, 1.3%와 극명한 차이를 보여, 위약 대비 나보타의 우수한 주름개선 효과를 입증했다. 시술 후 120일, 150일째에도 해당 응답 비율이 위약 대비 우월하게 나타났으며, 이런 결과는 미간주름 시술 후 증상개선을 평가하는 GAIS (Global Aesthetic Improvement Scales)에서도 동일하게 나타났다. 약물 관련 심각한 이상사례는 보고되지 않아 나보타의 안전성 또한 입증됐다.
미국 3상 임상의 연구 책임자이자 이번 논문의 제 1 저자인 케네스 비어 마이애미 대학 교수는 “이번 SCI급 논문 게재는 나보타의 안전성과 유효성을 다시 한번 입증한 것”이라며 “향후 보툴리눔 톡신 제품 선택의 기준이 될 수 있을 것으로 기대한다”고 말했다.
박성수 대웅제약 나보타 사업본부장은 “글로벌 임상결과에서 입증된 나보타의 유효성과 안전성이 권위 있는 국제학술지에 게재돼 나보타의 우수성을 전세계적으로 더욱 널리 알릴 수 있게 됐다”며 “앞으로도 다양한 기회를 통해 글로벌 브랜드로서의 위상을 더욱 공고히 다져나갈 것”이라고 설명했다.











![요즘 가요계선 '역주행'이 대세?…윤수일 '아파트'→키오프 '이글루'까지 [이슈크래커]](https://img.etoday.co.kr/crop/320/200/2099221.jpg)