[ASCO 2020] 367명 환자 추적결과 포스터 발표..오리지널과 동등한 안전성·효능 확인
삼성바이오에피스는 29일(현지시간) 열린 미국 임상종양학회(ASCO) 학술대회의 포스터 세션에 참여해 항암제 온트루잔트(Ontruzant, 허셉틴 바이오시밀러, 성분명 트라스트주맙)의 새로운 추적 임상 결과를 공개했다.
삼성바이오에피스는 임상 3상 이후 추적 관찰에 동의한 총 367명의 환자를 대상으로 온트루잔트와 오리지널 의약품의 효능 및 안전성 등을 비교 연구하고 있다. 총 추적 관찰 기간은 5년이며, 이번에 발표된 데이터는 그 중 53개월에 해당되는 최초 4년간의 수치를 집계한 것이다.
연구 결과에 따르면, 심장의 이상 기능을 확인할 수 있는 지표인 `좌심실 박출률(LVEF: Left Ventricular Ejection Fraction)` 수치가 저하된 환자는 온트루잔트 투여군 중 1명, 오리지널 의약품 투여군 중 2명으로 둘 다 낮은 수치를 보였다.
또 다른 안전성 지표인 `울혈성 심부전증(CHF: Congestive Heart Failure)` 관련된 이상 징후는 두 집단 모두에게서 발견되지 않았다.
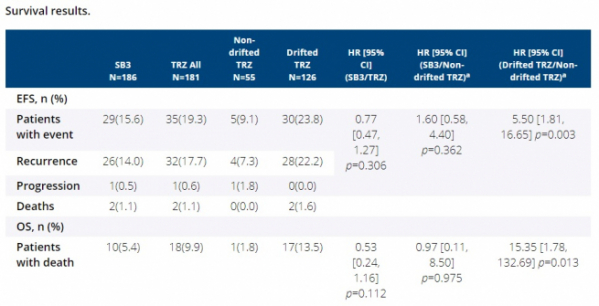
의약품 효능 측면에서의 연구 결과를 살펴보면, 치료 시작 후 심각한 부작용이나 재발, 전이 등이 발생하지 않고 생존하는 비율인 `무사건 생존율(EFS: Event-free survival)`은 온트루잔트 투여군에서 83.4%, 오리지널 의약품을 투여군에서 80.7%의 결과를 보였다(95 % CI 0.47, 1.27).
치료 후 일정 기간이 경과했을 때 환자가 생존하는 비율을 나타내는 `전체 생존율(OS: Overall survival)`은 온트루잔트 투여군에서 94.4%, 오리지널 의약품 투여군에서 89.6%의 수치를 보였다(95 % CI 0.24, 1.16).
한편, 삼성바이오에피스는 지난 4월 미국서 온트루잔트 출시를 통해 세계 최대 의약품 시장에서 항암제 판매에 본격 나섰다. 삼성바이오에피스는 미국 파트너사 머크(Merck)와의 협력을 강화함과 더불어 공급 역량, 품질관리 역량을 발휘해 시장 진입 활로를 뚫겠다는 전략이다.











![[컬처콕 플러스] 아일릿, 논란 딛고 다시 직진할 수 있을까?](https://img.etoday.co.kr/crop/320/200/2095915.jpg)