부작용·불신 부담에 신중한 태도 보여
전 세계가 고대했던 ‘옥토버 서프라이즈’가 물거품이 되게 생겼다. 신종 코로나바이러스 감염증(코로나19) 팬데믹 초기부터 불꽃 튀던 백신 개발 경쟁이 안전성 우려에 잇따라 좌초되면서 ‘10월 백신 출시설’은 말 그대로 ‘설(說)’에 그치게 됐다.
17일(현지시간) 파이낸셜타임스(FT)에 따르면 코로나19 백신 개발 경쟁에서 선두를 달리던 미국 제약업체 화이자는 전날 성명을 내고 “긴급 사용허가 신청은 11월 셋째 주 이후에 낼 것”이라고 밝혔다. 앨버트 불라 화이자 최고경영자(CEO)는 홈페이지에 공개한 서한에서 “백신이 안전하고 규제 기준을 만족한다는 확신을 해야 한다”며 “미국 식품의약국(FDA)이 최종 백신 접종 후 임상 참가자 절반에 대한 2개월간의 추적 데이터를 요구하고 있다”고 설명했다. 이어 “현재 투약 속도를 고려하면 11월 셋째 주 이후에나 이 기준에 도달할 것”이라고 덧붙였다.
앞서 도널드 트럼프 미국 대통령은 재선 전략으로 11월 3일 미국 대선 전 백신 접종을 시작하겠다고 공언했다. 트럼프 대통령의 말대로라면 10월 안에 백신이 출시되는 ‘옥토버 서프라이즈’가 실현되는 것이다. 하지만 백신 개발 선두 업체들이 잇따라 임상 시험을 중단한 데 이어 믿었던 화이자마저 대선 이후로 출시 일정을 연기하면서 트럼프 대통령의 계획에도 차질이 불가피하게 됐다.
화이자의 이날 발표는 최근 다른 제약업체들이 코로나19 백신 개발 경쟁에서 잇따라 탈락한 영향으로 풀이된다. 코로나19 백신 개발 경쟁은 3월부터 불이 붙었다. 현재 제약업체 10곳이 임상 시험의 최종 단계를 진행하고 있지만, 저마다 임상 중단과 일정 조정 등을 발표하며 연초에 보였던 속도감은 찾기 힘들다.
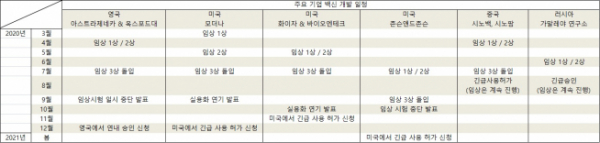
12일 존슨앤드존슨(J&J)은 임상 3상에 참가한 환자에게서 예기치 않은 질병이 나타나 6만 명 규모의 임상을 일시 중단하겠다고 밝혔다. 임상이 언제 재개될지는 미지수다. 모더나 역시 이달 안에 임상 시험을 종료할 계획이었지만, “11~12월 사이에 결과가 나올 것”이라고 번복했다. 영국 아스트라제네카는 지난달 8일 전 세계 임상 3상을 일시 중단했다가 4일 만에 규제 당국의 승인을 받아 임상 시험을 재개했다.
제약업체의 연이은 임상 중단은 졸속 개발에 따른 한계를 드러낸 것이다. 치료제는 감염자에게, 백신은 건강한 정상인에게 투여해야 하는 만큼 안전성이 특히 중요하다. 백신 개발에는 최소 3~5년이 걸리고, 신기술을 적용할 경우에는 10년 가까이 걸리는 것이 보통이다. 투여 후에는 부작용의 빈도와 종류, 예방 효과 등을 1~2년 동안 관찰해야 한다. 제약 업계에서는 “제약 업체의 생명선은 데이터로 증명하는 것”이라고 할 정도로 해당 과정이 필수다.
하지만 코로나19 백신 개발은 임상 시험에 할당한 시간이 2~3개월에 불과했다. 미국의 ‘워프 스피드 작전’ 등 각국 정부가 연내 상용화를 지원하는 과정에서 안전성보다 속도에 방점을 찍은 탓이다. 정부 쪽에선 코로나19 백신에 부작용이 나타날 경우 당국이 책임을 지겠다고 했지만, 기업으로선 신뢰성과 브랜드에 대한 타격을 우려할 수밖에 없다.
높아지는 불신에 부담을 느낀 제약업체는 부작용 등을 철저히 검증하는 것이 우선이라며 신중한 태도를 보이고 나섰다. 모더나와 화이자, 아스트라제네카 등 글로벌 제약업체 9곳은 지난달 8일 공동 성명을 내고 정치적 압력에 굴하지 않겠다는 선언까지 했다. 일본 니혼게이자이신문은 “코로나19 백신이 외교 전략으로도 사용될 수 있어 정치적 목적으로 전용되기 쉽다”며 “코로나19 투쟁은 정부와 기업 양쪽에 무거운 과제”라고 설명했다.











![요즘 가요계선 '역주행'이 대세?…윤수일 '아파트'→키오프 '이글루'까지 [이슈크래커]](https://img.etoday.co.kr/crop/320/200/2099221.jpg)