EU 집행위 결정만 남아
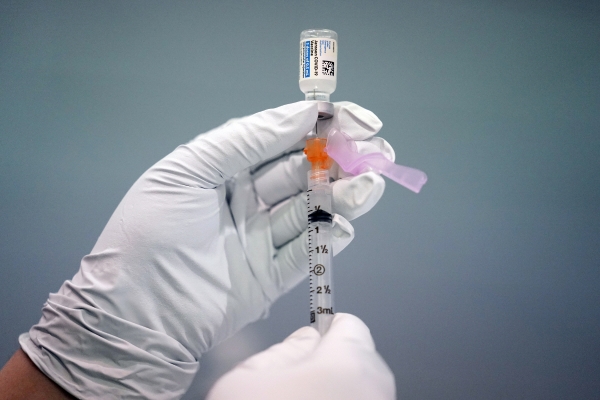
유럽의약품청(EMA)은 1일(현지시간) 오미크론 변이를 겨냥한 화이자와 모더나의 새로운 신종 코로나바이러스 감염증(코로나19) 백신의 유럽연합(EU) 내 판매 승인을 권고했다.
AFP통신에 따르면 EMA는 이날 성명을 내고 화이자와 모더나가 코로나19 신종변이 오미크론을 겨냥해 맞춤형으로 개발한 2가 백신의 판매 승인을 권고했다고 밝혔다.
이로써 해당 백신이 EU 역내에서 배포되기까지 유럽 행정부 격인 EU 집행위원회 최종 승인 절차만 남게 됐다. EMA가 오미크론 등 코로나19 하위변이를 겨냥한 2가 백신을 승인한 것은 이번이 처음이다. 앞서 미국 식품의약국(FDA)이 지난달 31일 두 백신에 대한 사용을 승인했다.
EU는 지금까지 미국 제약사 화이자-독일 바이오엔테크, 미국 모더나, 존슨앤드존슨(J&J) 제약 부문 계열사 얀센, 노바백스, 다국적 제약사 아스트라제네카, 발네바 등 6개 백신을 승인했다.
새 백신은 기존 코로나19 백신을 최소한 1차례 이상 접종받은 12세 이상에 대해 기존 접종을 받은 지 3개월이 지난 후 접종이 가능하다.
이번 결정은 이전에 널리 배포됐던 코로나 1가 백신에 대한 효과 및 안전성 관련 자료와 동물 실험 데이터를 바탕으로 내려졌다. EMA는 관련 연구를 토대로 화이자와 모더나의 새 백신은 기존 백신 접종자들에게 기존 코로나19와 오미크론에 대해 강력한 면역반응을 촉발하며 특히 오미크론에 대한 면역반응을 일으키는 데 더욱 효과적인 것으로 나타났다고 설명했다.
앞서 영국은 지난달 15일 모더나가 개발한 2가 백신 사용을 세계 최초로 승인했고, 스위스와 호주도 지난달 뒤를 이었다. 우리나라 식품의약품안전처는 지난 7월 20일 미크론 변이를 겨냥한 모더나의 코로나19 2가 백신에 대해 사전검토를, 지난달 29일에는 화이자의 코로나19 2가 백신에 대한 품목허가 심사에 착수했다.











![[정치대학] 美 대선, 막판까지 초박빙…당선자별 韓 영향은?](https://img.etoday.co.kr/crop/320/200/2098110.jpg)