국내 기업 최초 혈액제제 ‘알리글로(ALYGLO)’, 美 FDA 허가
GC녹십자가 세계 최대 의약품 시장 미국에 국내 기업 최초로 혈액제제를 선보인다. 오랜 꿈이던 미국 시장에 진입에 성공하면서 본격적으로 기업 가치를 끌어올릴 것으로 기대된다.
GC녹십자는 미국 식품의약국(FDA)으로부터 혈액제제 ‘알리글로(ALYGLO)’의 품목허가를 받았다고 18일 공시했다. 알리글로는 선천성 면역결핍증으로도 불리는 일차 면역결핍증(Primary Humoral Immunodeficiency)에 쓰이는 정맥투여용 면역글로불린 10% 제제이다.
혈액제제의 미국 FDA 품목허가는 GC녹십자의 숙원이었다. 회사는 2015년 면역글로불린 5% 제제로 FDA 품목허가를 신청했지만, 2016년과 2017년 제조공정 관련 자료를 요구받으면서 전략을 수정했다. 이에 면역글로불린 10% 제제로 다시 도전하고 코로나19 팬데믹으로 생산설비인 오창공장의 비대면 평가를 받았지만, 현장실사가 필요하단 이유로 지난해 2월 보완요구서한(CRL)을 받았다.
GC녹십자는 올해 4월 오창공장의 현장실사를 받고 생물학적제제 허가신청서(BLA)를 재차 제출했다. FDA가 내년 1월 13일(현지시간)로 회사 측에 알렸던 기한보다 약 1개월 빠르게 승인된 만큼, 현장실사 후 품목허가까지 일사천리로 이뤄졌단 평가다.
시장조사기관 마케팅 리서치 브루(Marketing Research Bureau)에 따르면 미국 면역글로불린 시장은 2022년 기준 104억 달러(약 13조 원)에 달하는 거대한 규모다. 특히 인구노령화로 면역질환이 늘면서 수요가 꾸준히 증가하고 있다.
GC녹십자는 미국법인 GC바이오파마USA를 통해 알리글로의 직판(직접 판매)에 나선다. 내년 하반기 출시해 5년간 3%의 시장을 점유하겠단 목표를 세웠다. 현재 시장 규모로 추정해도 3000억~4000억 원에 이르는 추가 매출이 가능하다.
회사 관계자는 “혈액제제는 전문 약국(Specialty pharmacy) 채널을 타깃하기 때문에 직판이 가장 효과적인 접근 방법”이라며 “미국 현지에서 공급이 모자란 상황인 만큼 수요가 꾸준할 것”이라고 설명했다.
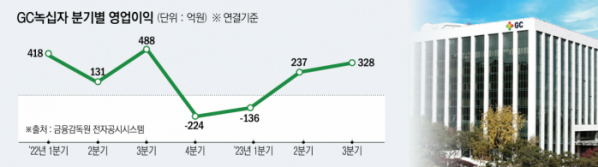
혈액제제의 미국 진출은 최근 주춤한 실적 흐름을 보이는 GC녹십자에게 반등의 기회가 될 것으로 기대된다. 올해 3분기까지 누적 매출은 1조2217억 원, 영업이익은 428억 원을 기록해 전년동기 대비 각각 6.0%, 58.7% 감소했다. 회사는 내년 초까지 백여 개 팀을 통폐합해 조직 규모를 10% 감축하고 희망퇴직을 시행하는 구조조정을 진행 중이다.
중장기적인 성장을 위해 GC녹십자는 다방면으로 활로를 찾고 있다. 대표 사업인 혈액제제는 미국 직판 외에도 플랜트 수출에 나섰다. 올해 6월 인도네시아 보건복지부로부터 혈액제제 플랜트 건설 및 기술 이전 관련 사업권을 승인받고, 약 6개월 만인 이달 6일 인도네시아 자카르타 인근에서 현지 최초 혈액제제 공장 착공식을 진행했다. 2027년 가동 예정으로 연간 최대 40만 리터의 원료 혈장을 처리할 수 있다.
차세대 신약개발 플랫폼으로는 메신저리보핵산(mRNA)을 선택했다. mRNA 독감백신과 희귀질환인 숙신알데히드탈수소효소결핍증(SSADHD) 치료제를 개발하고 있다. 또한, 전남 화순 백신 공장에 파일럿 규모의 mRNA 생산시설을 구축해 임상시험용 의약품 생산을 시작으로 추후 위탁생산(CMO) 사업까지 영역을 확장할 계획이다.










![[정치대학] 美 대선, 막판까지 초박빙…당선자별 韓 영향은?](https://img.etoday.co.kr/crop/320/200/2098110.jpg)