연세대 의대 연구진 “신장 줄기세포 표지자 ‘Lrig1’, 기존 치료제 대비 안전성 높아”

국내 연구진이 손상된 신장을 재생시키는 줄기세포 표지자 발굴에 성공했다.
남기택 연세대 의과대학 의생명과학부 교수와 이유라 박사 연구팀은 ‘Lrig1 신장 내재성 줄기세포’를 손상된 신장에 주입했을 때 재생 효과가 나타났다고 14일 밝혔다.
이번 연구 결과는 국제학술지 ‘미국신장내과학회지(Journal of the American Society of Nephrology, IF 13.6)’에 게재됐다.
대한신장학회에 따르면 국내 말기콩팥병 발병률은 2022년 기준 인구 백만명 당 360.2명으로 2010년에 비해 2배 이상 증가했다. 말기콩팥병의 치료에는 혈액투석이나 복막투석, 신장이식 등이 있다. 국내 등록된 말기콩팥병 환자 중 혈액투석 환자는 84%, 복막투석 환자는 6%, 신장이식 환자는 11%로 집계됐다.
투석 치료는 환자의 삶의 질을 크게 떨어뜨린다. 신장이식은 대기기간이 5~7년으로 길고, 이식을 받더라도 면역억제제로 인한 부작용이 발생할 수 있다. 투석과 이식의 한계를 극복하기 위해 줄기세포를 활용한 세포치료제의 개발과 적용에 관한 연구가 진행되고 있다.
지금까지의 연구는 역분화 줄기세포를 이용해 신장 세포를 유도하는 세포치료 전략이 주를 이뤘다. 하지만 분화 조절에 실패했을 때 종양 발생 위험이 있어 말기콩팥병 치료를 위한 세포치료제로서 적합성에 의문이 있었다.
이에 신장 내 존재하는 내재성 줄기세포 표지자를 이용해 특정 세포를 분리하고 이를 신장 세포로 분화를 유도해 손상된 신장에 이식하는 세포치료제가 대안으로 제시되고 있다. 지금까지 손상된 신장을 재생할 수 있는 조직 내 줄기세포 존재 여부가 불분명해 관련 연구는 답보상태이다.
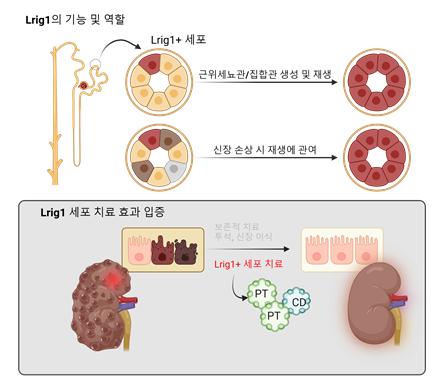
연구팀은 신장 손상의 시작 부위인 근위세뇨관을 표적으로 연구한 결과 Lrig1 유전자를 신장 줄기세포 표지자로 제시했다. Lrig1 세포는 위나 피부, 소장 등 다양한 조직에서 장기간 생존하며 조직 재생에 관여하는 것으로 알려졌다.
연구팀은 형질전환 마우스 모델을 활용해 생애 전 주기에 걸쳐 신장 발달과정 동안 Lrig1 세포를 추적했다. 마우스 배아 단계 13.5일부터 성체까지 신장 피질에서 Lrig1의 발현이 나타났다.
신장에서 분리한 Lrig1 발현세포를 오가노이드로 배양한 상태에서도 단일 Lrig1+ 세포는 체외에서 장기간 증식이 가능했고, 근위세뇨관과 집합관 계통의 세포로도 분화했다. Lrig1을 발현하는 세포를 단일 세포 RNA 시퀀싱 분석한 결과 줄기세포의 특성을 반영한 유전자가 관측돼, Lrig1+ 세포가 내재성 줄기세포로서의 가능성이 분자생물학적 수준에서 입증됐다.
마우스 신장에서 Lrig1 분화 세포를 추적한 결과, Lrig1 유래 근위세뇨관 세포들이 줄기세포 증식과 관련된 유전자들을 풍부하게 발현해 신장 근위세뇨관과 집합관 구조형성에 기여하는 것으로 나타났다. 이를 통해 Lrig1과 그 분화 세포들이 신장 조직에서 장기간 생존하며 조직의 항상성과 재생에 관여하는 줄기세포임을 확인했다.
연구 결과를 검증하기 위해 급성 신장 손상 마우스 모델을 구축해 Lrig1 세포를 추적했을 때에도 Lrig1과 분화 세포들이 실제로 조직 재생에 관여했다.
연구팀은 Lrig1 기반의 세포치료제 적용 가능성 확인을 위해 Lrig1 유래 오가노이드를 마우스 급성 신장 손상 모델에 이식해 치료 능력을 평가했다.
신장 손상 시, 신장이 혈액에서 노폐물을 적절히 제거하지 못해 혈액요소질소(BUN)와 크레아티닌 수치가 정상 대비 약 2~10배 이상 증가하게 된다. Lrig1 유래 오가노이드를 이식한 신장 손상 마우스의 혈액에서 BUN과 크레아티닌의 농도를 확인한 결과, 혈중 BUN 및 크레아티닌 농도가 정상 수준으로 회복됐으며, 신장 손상 지표인 KIM1 단백질의 발현도 관찰되지 않았다.
남 교수는 “마우스 신장 내 Lrig1 세포의 특성은 사람 유래 Lrig1 세포에서도 유사해, 향후 사람 유래 Lrig1 세포의 분리 배양을 통해 기존의 줄기세포 기반 세포치료제보다 안정적인 분화가 가능한 손상 신장 치료제로 적용이 가능할 것”이라고 말했다.











![[컬처콕 플러스] 아일릿, 논란 딛고 다시 직진할 수 있을까?](https://img.etoday.co.kr/crop/320/200/2095915.jpg)