아스트라제네카 코로나19 백신, 검증 자문단 회의 31일 열려…결과는 2월 1일 공개
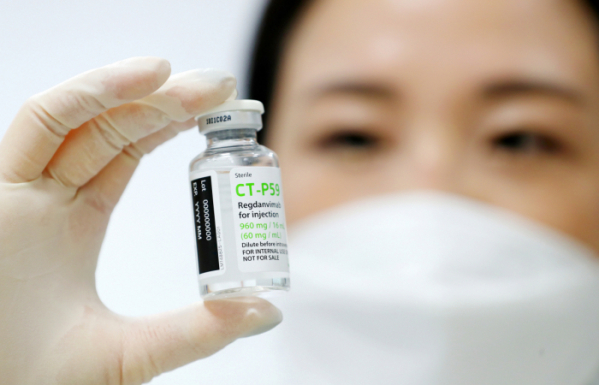
셀트리온의 코로나19 항체치료제에 대한 2차 자문 결과가 27일 공개된다.
식품의약품안전처는 셀트리온이 조건부 허가를 신청한 코로나19 항체치료제 ‘렉키로나주’(성분명 레그단비맙·CT-P59)의 2상 임상시험 자료에 대해 27일 법정 자문기구인 ‘중앙약사심의위원회’에 자문을 받고, 그 결과를 당일 공개할 예정이라고 21일 밝혔다.
식약처는 코로나19 백신과 치료제를 허가하기 전 △검증 자문단 △중앙약사심의위원회 △최종점검위원회 등 3중의 자문 절차를 거쳐 심사한다. 중앙약사심의위원회 자문 전 18일 발표된 검증 자문단 회의에서는 렉키로나주의 효과성을 인정했지만 추가 검증이 필요하다고 판단했고 결론적으로 식약처에 조건부 허가를 권고했다.
식약처는 20일 셀트리온에 렉키로나주와 관련해 아직 제출되지 않은 품질자료 일부 등에 대한 자료 제출을 요청했고, 제출되는 대로 심사를 계속 진행할 예정이다. 이후 심사 결과를 종합해 ‘중앙약사심의위원회’에서 신청 품목의 안전성, 효과성, 허가 시 고려해야 할 사항 등에 대해 27일 자문을 받는다.
한편 자문에 앞서 식약처는 ‘렉키로나주’에 대한 임상시험 대상자의 안전과 시험결과의 신뢰성 등 임상시험 전반에 걸친 규정 준수 여부를 12~15일 4일간 임상시험실시기관(의료기관)에 대한 실태조사, 서류검토 등을 통해 확인했다.
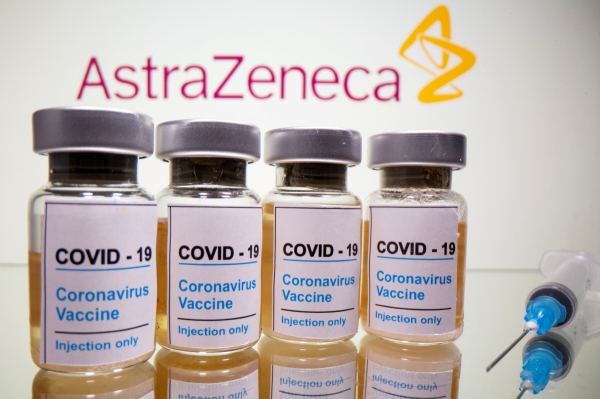
아스트라제네카 코로나19 백신에 대한 검증 자문단 회의는 31일 열린다.
식약처는 한국아스트라제네카가 품목허가 신청한 ‘아스트라제네카코비드-19백신주’에 대한 임상시험 자료와 관련해 외부 전문가들이 참여하는 ‘코로나19 백신 안전성ㆍ효과성 검증 자문단’ 회의는 31일 연다고 밝혔다. 회의 결과는 2월 1일 공개 예정이다.
자문단은 감염내과 중심의 임상전문가, 비임상, 품질분야에 전문지식과 경험이 풍부한 외부 전문가로 구성되고, 신청품목의 안전성과 효과성, 임상적 의의, 대상환자의 적정성 등에 대해 자문할 예정이다.
앞서 식약처는 아스트라제네카 코로나19 백신과 관련해 제조소에 대한 실태조사를 마쳤다. 이후 지난 14일 비임상ㆍ임상시험 자료와 품질자료 등 심사에 필요한 자료를 추가로 요청했고, 자료가 제출되는 대로 예방효과, 신청한 용법ㆍ용량의 타당성, 안전성 등에 대해 검토하고 국가출하승인을 위한 품질분야 심사에 집중할 예정이다.











![[컬처콕 플러스] '아파트' 대박난 로제, 제니·로사와 다른 점은?](https://img.etoday.co.kr/crop/320/200/2099568.jpg)