국산 항암제 첫 FDA 승인…항암제 시장 중 가장 큰 폐암 타깃

유한양행이 개발한 3세대 폐암치료제 ‘렉라자(성분명 레이저티닙)’가 미국 식품의약국(FDA) 문턱을 넘었다. 기존 글로벌 표준치료제인 오시머티닙(제품명 타그리소)과 비교했을 때 뒤지지 않는 효능과 안전성을 확보한 만큼 국내 첫 블록버스터 신약으로서의 가능성도 점쳐지고 있다.
21일 본지 취재를 종합하면 FDA로부터 승인받은 국산 신약은 렉라자를 포함해 총 9개다. 2003년 LG화학의 항생제 ‘팩티브’를 필두로 2014년 동아ST의 항생제 ‘시벡스트로’, 2016년 SK케미칼의 혈우병 치료제 ‘앱스틸라’, 2019년 SK바이오팜의 수면장애 치료제 ‘수노시’와 뇌전증 치료제 ‘엑스코프리’ 등이 FDA 허가를 받았다.
이어 2022년 한미약품의 호중구감소증 치료제 ‘롤론티스’, 2023년 셀트리온의 자가면역질환 치료제 ‘짐펜트라’와 GC녹십자의 면역결핍증 혈액제제 ‘알리글로’가 FDA 문턱을 넘었고, 뒤를 이어 19일(현지시간) 유한양행의 ‘렉라자’가 FDA 승인을 받았다.
그동안 FDA에서 승인받은 국산 신약 가운데 연간 매출 1조 원 이상의 글로벌 블록버스터 신약은 없었다. 렉라자는 국산 항암제 최초로 FDA 승인을 받았고, 전체 항암제 시장 중 가장 큰 폐암을 타깃하고 있어 블록버스터로서의 가능성이 큰 편이다.
시장조사기관 이벨류에이트파마(Evaluate pharma)에 따르면 2023년 기준 글로벌 폐암 치료제 시장은 전체 항암제 시장의 18%에 해당하는 348억 달러(45조6000억 원)를 기록했다. 이는 전 세계 항암제 시장 중 가장 큰 부분을 차지하는 수치다. 또한 폐암 치료제 시장은 연평균 9% 성장해 2028년 시장 규모 582억 달러(76조6000억 원)로 확대될 것으로 전망된다.
특히 비소세포폐암은 전체 폐암의 80~85%를 차지한다. 비소세포폐암 환자 수가 압도적으로 많아 치료제 시장 역시 비소세포폐암이 전체 폐암 치료제 시장의 대부분을 차지하고 있다.
비소세포폐암에서 가장 흔한 유전자 돌연변이는 상피세포 성장인자 수용체(EGFR) 돌연변이로, 비소세포폐암 표적항암제 시장에서도 EGFR 표적항암제 시장 규모가 제일 크다. 비소세포폐암 EGFR 돌연변이는 인종에 따라 다르게 나타난다. 의학계에서는 서양인의 경우 5~15%, 아시아인의 경우 40~55%가 EGFR 돌연변이라고 알려져 있다.
렉라자가 기대를 받은 이유는 존슨앤드존슨(J&J)의 이중항체 리브리반트(성분명 아미반타맙)와 병용요법으로 ‘EGFR 엑손 19 결실’ 또는 ‘엑손 21 L858R 치환 변이’가 확인된 국소 진행성 또는 전이성 비소세포폐암 성인 환자의 1차 치료제로 FDA 승인을 받아서다.
현재 오시머티닙이 EGFR 변이치료제 시장의 절반 이상을 차지하고 있다. 이번 승인으로 그동안 오시머티닙 치료에만 의존해야 했던 환자들에게 새로운 치료법이 확대된 셈이다. 렉라자·리브리반트 병용요법이 기존 치료법 대비 효과가 있음을 확인한 만큼 시장 점유율을 앞지를 것이라는 기대를 모으고 있다.
이번 FDA 허가는 1074명의 환자를 대상으로 진행한 ‘마리포사(MRIPOSA)’ 임상3상 연구를 토대로 이뤄졌다.
해당 임상에 따르면 렉라자와 존슨앤드존슨(J&J)의 이중항체 리브리반트(성분명 아미반타맙) 병용요법이 오시머티닙(제품명 타그리소) 단독요법 대비 질병 진행 또는 사망 위험을 30% 감소시켰다. 무진행 생존기간(PFS)은 오시머티닙의 16.6개월보다 긴 23.7개월로 나타났고 위축된 암의 크기가 유지되는 ‘반응 지속기간(DOR)’도 25.8개월로 오시머티닙의 16.8개월보다 9개월 길었다.
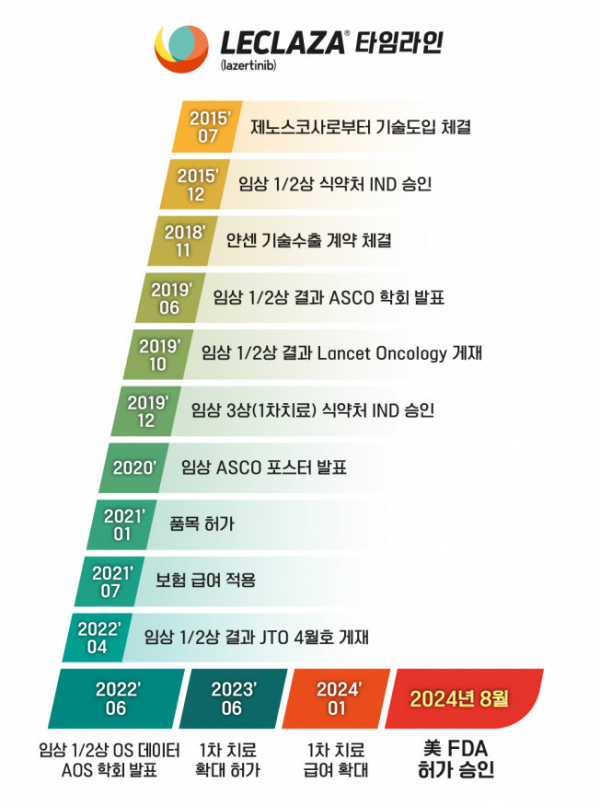
렉라자는 국내 바이오기업 오스코텍이 개발해 2015년 유한양행이 기술을 도입한 국산 신약이다. 유한양행은 임상을 거쳐 2018년 J&J의 자회사인 얀센에 렉라자의 글로벌 개발·판매 권리(국내 제외)를 12억5500만 달러(약 1조6000억 원)에 다시 기술수출했다.
국내에서는 2021년 식품의약품안전처로부터 국산 신약 31호로 허가받았으며 지난해 6월 국내 비소세포폐암 1차 치료제로 허가가 확대됐다.
J&J는 렉라자와 리브리반트의 병용요법으로 연간 50억 달러(약 6조7725억 원)의 매출을 올릴 것으로 기대하고 있다. 유한양행은 이번 FDA 허가로 약 820억 원 규모의 마일스톤(단계별 기술료)을 수령할 전망이다. 향후 제품 판매가 본격화되면 최소 10% 이상의 제품 판매 로열티도 받게 된다.









![[컬처콕 플러스] 아일릿, 논란 딛고 다시 직진할 수 있을까?](https://img.etoday.co.kr/crop/320/200/2095915.jpg)